摘要:PGK1的酶在脑细胞化学能的产生中起着意想不到的关键作用。
根据威尔康奈尔医学院的研究人员领导的一项临床前研究,一种名为PGK1的酶在脑细胞化学能的产生中起着意想不到的关键作用。研究人员发现,增强它的活性可能有助于大脑抵抗可能导致帕金森病的能量不足。
这项研究发表在8月21日的《科学进展》杂志上,证明了PGK1是一种“限速”酶,在多巴胺神经元的输出信号分支或轴突中产生能量,而多巴胺神经元在帕金森病中受到影响。这意味着即使是适度的提高PGK1的活性,在低燃料条件下也能对恢复神经元的能量供应产生巨大的影响——研究人员表明,这可以防止轴突功能障碍和退化,通常在帕金森病的动物模型中看到。

图1 磷酸甘油酸激酶是帕金森病驱动的神经元代谢缺陷的核心杠杆点
“我们的研究结果表明,PGK1确实可以以我们没有预料到的方式对帕金森病产生重大影响,我非常乐观地认为,这一系列研究有可能产生新的帕金森病治疗方法。”该研究的资深作者、威尔康奈尔医学院生物化学三机构教授蒂莫西·瑞安博士说。
这项研究的第一作者是亚历山德罗斯·科科托斯博士,他是瑞安实验室的博士后研究员。
帕金森氏症折磨着大约100万美国人,是仅次于阿尔茨海默氏症的第二大常见神经退行性疾病。这种疾病会袭击产生多巴胺的关键神经元群,最初会削弱它们的突触,或与其他神经元的连接点,最终导致它们死亡。这种疾病的症状和体征包括运动障碍、睡眠问题和最终的痴呆。目前的治疗方法解决症状,但不能停止疾病进程。
几十年来,各种各样的研究都指出,帕金森氏症是一种影响能量需求非常高的神经元的疾病,神经元能量供应不足是导致帕金森氏症的一个因素。即便如此,研究人员仍缺乏一个与能量相关的疾病治疗目标。
对PGK1的新关注源于最近的研究表明,美国食品和药物管理局(Food and Drug administration)批准的用于治疗前列腺肥大的药物特拉唑嗪(terazosin)也能增强PGK1的能量产生活性,并在多种帕金森病动物模型中具有有益作用。然而,在这些研究中,terazosin促进PGK1活性的能力相当弱,其作用机制尚不确定。一项对人类的回顾性研究进一步证明了该药物在增强神经保护方面的作用,该研究表明,特拉唑嗪显著降低了患帕金森病的风险。
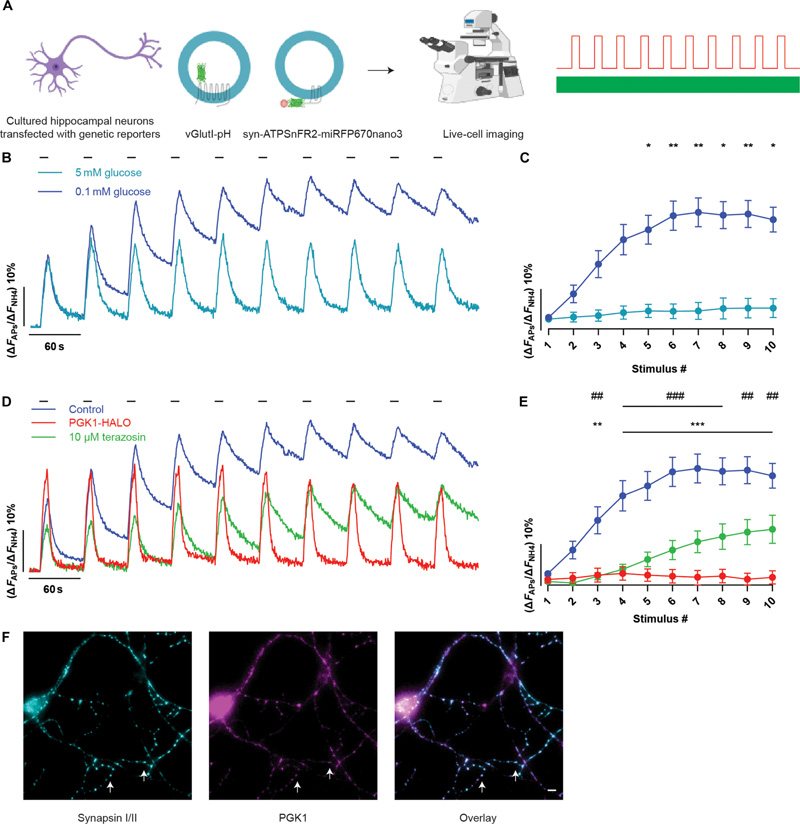
图2 HEK293细胞中不同激动剂的cAMP剂量反应
“制药公司一直怀疑这种PGK1的微弱增强能否解释帕金森模型中的这些益处,”莱恩博士说,他也是威尔康奈尔医学院(Weill Cornell Medicine)麻醉学生物化学教授。
在这项新研究中,团队通过敏感的检测方法解决了这个问题,这些检测方法阐明了PGK1在神经元中作为能量生产者的作用。研究人员发现,这种作用是如此重要,以至于当葡萄糖水平较低时,即使是对PGK1活性的小幅提升,比如特拉唑嗪,也足以保持轴突的功能。葡萄糖是PGK1帮助转化为基本化学能单位的。实验包括由已知的帕金森相关基因突变引起的低血糖情况。
研究小组还发现了一种名为DJ-1的蛋白质,它的突变导致的损伤是帕金森病的另一种已知遗传原因。DJ-1是一种“伴侣”,被认为通过阻止有害蛋白质聚集来保护神经元。然而,研究小组发现,DJ-1作为PGK1的亲密伙伴,发挥着意想不到的能量供应作用,并且确实是PGK1增强的必要条件。
瑞安博士认为,研究结果进一步证实了这样一种理论,即由衰老、遗传和环境因素导致的最脆弱的多巴胺神经元的能量供应不足是帕金森病的一个普遍的早期驱动因素,适度增强一种酶PGK1的活性,可能就足以扭转这种缺陷,阻止疾病的发展。
“现在我可以说,我有信心这种酶应该是我们的目标,”瑞安博士说。“考虑到terazosin在预防人类帕金森氏症方面的积极影响,以及这种药物从未优化过增强PGK1的事实,考虑到新药可能的临床影响,与terazosin相比,可以更有效和有选择性地增强PGK1活性,这是令人兴奋的。”
参考资料
[1] Phosphoglycerate kinase is a central leverage point in Parkinson’s disease–driven neuronal metabolic deficits
摘要:PGK1的酶在脑细胞化学能的产生中起着意想不到的关键作用。
根据威尔康奈尔医学院的研究人员领导的一项临床前研究,一种名为PGK1的酶在脑细胞化学能的产生中起着意想不到的关键作用。研究人员发现,增强它的活性可能有助于大脑抵抗可能导致帕金森病的能量不足。
这项研究发表在8月21日的《科学进展》杂志上,证明了PGK1是一种“限速”酶,在多巴胺神经元的输出信号分支或轴突中产生能量,而多巴胺神经元在帕金森病中受到影响。这意味着即使是适度的提高PGK1的活性,在低燃料条件下也能对恢复神经元的能量供应产生巨大的影响——研究人员表明,这可以防止轴突功能障碍和退化,通常在帕金森病的动物模型中看到。

图1 磷酸甘油酸激酶是帕金森病驱动的神经元代谢缺陷的核心杠杆点
“我们的研究结果表明,PGK1确实可以以我们没有预料到的方式对帕金森病产生重大影响,我非常乐观地认为,这一系列研究有可能产生新的帕金森病治疗方法。”该研究的资深作者、威尔康奈尔医学院生物化学三机构教授蒂莫西·瑞安博士说。
这项研究的第一作者是亚历山德罗斯·科科托斯博士,他是瑞安实验室的博士后研究员。
帕金森氏症折磨着大约100万美国人,是仅次于阿尔茨海默氏症的第二大常见神经退行性疾病。这种疾病会袭击产生多巴胺的关键神经元群,最初会削弱它们的突触,或与其他神经元的连接点,最终导致它们死亡。这种疾病的症状和体征包括运动障碍、睡眠问题和最终的痴呆。目前的治疗方法解决症状,但不能停止疾病进程。
几十年来,各种各样的研究都指出,帕金森氏症是一种影响能量需求非常高的神经元的疾病,神经元能量供应不足是导致帕金森氏症的一个因素。即便如此,研究人员仍缺乏一个与能量相关的疾病治疗目标。
对PGK1的新关注源于最近的研究表明,美国食品和药物管理局(Food and Drug administration)批准的用于治疗前列腺肥大的药物特拉唑嗪(terazosin)也能增强PGK1的能量产生活性,并在多种帕金森病动物模型中具有有益作用。然而,在这些研究中,terazosin促进PGK1活性的能力相当弱,其作用机制尚不确定。一项对人类的回顾性研究进一步证明了该药物在增强神经保护方面的作用,该研究表明,特拉唑嗪显著降低了患帕金森病的风险。

图2 HEK293细胞中不同激动剂的cAMP剂量反应
“制药公司一直怀疑这种PGK1的微弱增强能否解释帕金森模型中的这些益处,”莱恩博士说,他也是威尔康奈尔医学院(Weill Cornell Medicine)麻醉学生物化学教授。
在这项新研究中,团队通过敏感的检测方法解决了这个问题,这些检测方法阐明了PGK1在神经元中作为能量生产者的作用。研究人员发现,这种作用是如此重要,以至于当葡萄糖水平较低时,即使是对PGK1活性的小幅提升,比如特拉唑嗪,也足以保持轴突的功能。葡萄糖是PGK1帮助转化为基本化学能单位的。实验包括由已知的帕金森相关基因突变引起的低血糖情况。
研究小组还发现了一种名为DJ-1的蛋白质,它的突变导致的损伤是帕金森病的另一种已知遗传原因。DJ-1是一种“伴侣”,被认为通过阻止有害蛋白质聚集来保护神经元。然而,研究小组发现,DJ-1作为PGK1的亲密伙伴,发挥着意想不到的能量供应作用,并且确实是PGK1增强的必要条件。
瑞安博士认为,研究结果进一步证实了这样一种理论,即由衰老、遗传和环境因素导致的最脆弱的多巴胺神经元的能量供应不足是帕金森病的一个普遍的早期驱动因素,适度增强一种酶PGK1的活性,可能就足以扭转这种缺陷,阻止疾病的发展。
“现在我可以说,我有信心这种酶应该是我们的目标,”瑞安博士说。“考虑到terazosin在预防人类帕金森氏症方面的积极影响,以及这种药物从未优化过增强PGK1的事实,考虑到新药可能的临床影响,与terazosin相比,可以更有效和有选择性地增强PGK1活性,这是令人兴奋的。”
参考资料
[1] Phosphoglycerate kinase is a central leverage point in Parkinson’s disease–driven neuronal metabolic deficits



